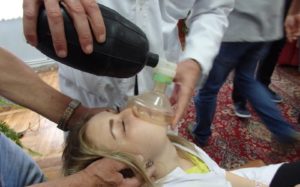
Признаки и симптомы поражения синильной кислотой (hcn)
Содержание:
Химические свойства
Очень слабая одноосновная кислота: её константа диссоциации Ka = 1,32⋅10−9, pKa = 8,88 (при 18 °C). Образует с металлами соли — цианиды. Взаимодействует с оксидами и гидроксидами щелочных и щёлочноземельных металлов.
Пары синильной кислоты горят на воздухе фиолетовым пламенем с образованием Н2О, СО и N2. Температура самовоспламенения в воздухе 538 °C. Температура вспышки −18 °C. Взрывоопасная концентрация паров HCN в воздухе 4,9—39,7%.
В смеси кислорода со фтором горит с выделением большого количества тепла:
- 2HCN+O2+F2→2HF+2CO+N2+1020{\displaystyle {\mathsf {2HCN+O_{2}+F_{2}\rightarrow 2HF+2CO+N_{2}+1020}}} кДж.
Синильная кислота широко применяется в органическом синтезе. Она реагирует с карбонильными соединениями, образуя циангидрины:
- RR′C=O+HCN→RR′C(OH)CN.{\displaystyle {\mathsf {RR’C\!=\!O+HCN\rightarrow RR’C(OH)CN}}.}
С хлором, бромом и иодом прямо образует циангалогениды:
- X2+HCN→XCN+HX.{\displaystyle {\mathsf {X_{2}+HCN\rightarrow XCN+HX}}.}
С галогеналканами — нитрилы (реакция Кольбе):
- RX+HCN→R−CN+HX.{\displaystyle {\mathsf {RX+HCN\rightarrow R\!-\!CN+HX}}.}
С алкенами и алкинами реагирует, присоединяясь к кратным связям:
- HCN+CH≡CH→Cu+CH2=CHCN.{\displaystyle {\mathsf {HCN+CH\!\equiv \!CH{\xrightarrow {Cu^{+}}}CH_{2}\!=\!CHCN}}.}
- HCN+CH2=CH2 →PdAl2O3 CH3CH2CN.{\displaystyle {\mathsf {HCN+CH_{2}\!=\!CH_{2}\ {\xrightarrow {Pd/Al_{2}O_{3}}}\ CH_{3}CH_{2}CN}}.}
- HCN+RCH=NH→Cu+RCH(NH2)CN.{\displaystyle {\mathsf {HCN+RCH\!=\!NH{\xrightarrow {Cu^{+}}}RCH(NH_{2})CN}}.}
Легко полимеризуется в присутствии основания (часто со взрывом). Образует аддукты, например, HCN-CuCl.
При разложении водой даёт формиат аммония, либо формамид
HCN+2H2O⟶HCOONH4{\displaystyle {\ce {HCN + 2H2O -> HCOONH4}}}
HCN+H2O⟶HCONH2{\displaystyle {\mathsf {HCN+H_{2}O\longrightarrow HCONH_{2}}}}
Профилактические мероприятия
 Чтобы не подвергаться действию цианистоводородной кислоты и избежать тяжёлых последствий её воздействия, необходимо:
Чтобы не подвергаться действию цианистоводородной кислоты и избежать тяжёлых последствий её воздействия, необходимо:
- неукоснительно следовать требованиям техники безопасности, при необходимости использовать противогаз;
- регулярно проветривать помещение после работы с токсичными веществами (дератизация, дезинсекция);
- постоянный контроль уровня вредных веществ на территории предприятия;
- по возможности использовать механизированный труд при работе с опасными веществами;
- следить за исправностью оборудования;
- личная гигиена;
- строгий отбор сотрудников по состоянию здоровья на предприятия с вредными условиями труда.
Каждого человека, который собирается работать в условиях вероятного воздействия цианидов, необходимо проинформировать, какой должна быть первая помощь пострадавшему при поражении синильной кислотой. От этого зависит жизнь самого человека и людей, которые работают рядом с ним.
В домашних условиях самостоятельное использование средств, содержащих синильную кислоту и её соли очень опасно. При этом можете пострадать вы и ваши близкие.
Физические свойства
Смешивается во всех соотношениях с водой, этанолом, диэтиловым эфиром. Смешивается также со многими другими спиртами и эфирами, ароматическими углеводородами и тетрахлоруглеродом.
Молекула HCN имеет линейное строение с межатомными расстояниями H—C 0,1064 нм и C≡N 0,1156 нм и сильно полярна (электрический дипольный момент μ = 0,992⋅10−29 Кл·м).
Безводный цианистый водород является сильно ионизирующим растворителем, растворённые в нём электролиты хорошо диссоциируют на ионы. Его относительная диэлектрическая проницаемость при 25 °C равна 106,8 (выше, чем у воды). Это обусловлено линейной ассоциацией полярных молекул HCN за счёт образования водородных связей.
Температура плавления −13,29 °C, кипения +25,65 °C. Плотность 0,71618 г/см3 при 0 °C, 0,68708 г/см3 при 0 °C.
Критическое давление 4,95 МПа, критическая температура +183,5 °C, критическая плотность 0,195 г/см3.
Коэффициент преломления nD = 1,26136 (20 °C).
Энтальпия образования 132 кДж/моль, энтальпия плавления 8,41 кДж/моль, энтальпия испарения 25,2 кДж/моль. Энтальпия сгорания −663 кДж/моль. Энтропия 201,71 Дж/(моль·К) (при 298 К).
Динамическая вязкость 0,183 мПа·с, кинематическая вязкость 17,78 мН/м.
Удельное электрическое сопротивление жидкой синильной кислоты 105 Ом·м.
Твёрдая синильная кислота при нормальном давлении существует в двух кристаллических модификациях. При температуре ниже −102,78°C образует кристаллы ромбической сингонии, пространственная группа I2mm, параметры ячейки a = 0,413 нм, b = 0,485 нм, c = 0,434 нм, Z = 2. Выше этой температуры переходит в кристаллы тетрагональной сингонии, пространственная группа I4mm, параметры ячейки a = 0,463 нм, c = 0,434 нм, Z = 2.
Охрана труда
ПДК в воздухе рабочей зоны равна 0,3 мг/м3 (максимально-разовая). По данным при опасной концентрации люди скорее всего не почувствуют запаха; а согласно порог восприятия запаха может быть 5,6 мг/м3. Поэтому использование широко распространённых в сочетании с «заменой по появлении запаха под маской» (как это почти всегда рекомендуется в РФ поставщиками СИЗОД) приведёт к чрезмерному воздействию синильной кислоты на, по крайней мере, часть работников — из-за запоздалой замены противогазных фильтров. Для защиты от этого вещества следует использовать значительно более эффективные технологии и средства коллективной защиты.
Соли
Основная статья: Цианиды
Соли синильной кислоты называются цианидами. Все цианиды, как и сама кислота, очень ядовиты. Цианиды подвержены сильному гидролизу. При хранении водных растворов цианидов при доступе диоксида углерода они разлагаются:
- KCN+H2O+CO2⟶HCN+KHCO3{\displaystyle {\mathsf {KCN+H_{2}O+CO_{2}\longrightarrow HCN+KHCO_{3}}}}
- KCN+2H2O⟶NH3+HCOOK{\displaystyle {\mathsf {KCN+2H_{2}O\longrightarrow NH_{3}+HCOOK}}}
Ион CN− (изоэлектронный молекуле СО) входит как лиганд в большое число комплексных соединений d-элементов. Комплексные цианиды в растворах очень стабильны.
Цианиды тяжёлых металлов термически неустойчивы; в воде, кроме цианида ртути (Hg(CN)2), нерастворимы. При окислении цианиды образуют соли — цианаты:
- 2KCN+O2⟶2KOCN{\displaystyle {\mathsf {2KCN+O_{2}\longrightarrow 2KOCN}}}
Многие металлы при действии избытка цианида калия или цианида натрия дают комплексные соединения, что используется, например, для извлечения золота и серебра из руд:
- 8NaCN+4Au+O2+2H2O⟶4NaAu(CN)2+4NaOH{\displaystyle {\mathsf {8NaCN+4Au+O_{2}+2H_{2}O\longrightarrow 4Na+4NaOH}}}
Биологическая роль
Показано, что нейроны способны вырабатывать эндогенную синильную кислоту (цианистый водород, HCN) после их активации эндогенными или экзогенными опиоидами и что образование нейронами эндогенной синильной кислоты повышает активность NMDA-рецепторов и, таким образом, может играть важную роль в передаче сигнала между нейронами (нейротрансмиссии). Более того, образование эндогенного цианида оказалось необходимым для проявления в полном объёме анальгетического действия эндогенных и экзогенных опиоидов, а вещества, снижающие образование свободной HCN, оказались способны уменьшать (но не полностью устранять) анальгетическое действие эндогенных и экзогенных опиоидов. Выдвинуто предположение, что эндогенная синильная кислота может являться нейромодулятором.
Известно также, что стимуляция мускариновых холинорецепторов клеток феохромоцитомы в культуре повышает образование ими эндогенной синильной кислоты, однако стимуляция мускариновых холинорецепторов ЦНС в живом организме крысы приводит, наоборот, к снижению образования эндогенной синильной кислоты.
Также показано, что синильная кислота выделяется лейкоцитами в процессе фагоцитоза и способна убивать патогенные микроорганизмы.
Возможно, что вазодилатация, вызываемая нитропруссидом натрия, связана не только с образованием окиси азота (механизм, общий для действия всех сосудорасширяющих препаратов группы нитратов, таких как нитроглицерин, нитросорбид), но и с образованием цианида. Возможно, что эндогенный цианид и образующийся при его обезвреживании в организме тиоцианат играют роль в регуляции функций сердечно-сосудистой системы, в обеспечении вазодилатации и являются одними из эндогенных антигипертензивных веществ.
Физические свойства
Смешивается во всех соотношениях с водой, этанолом, диэтиловым эфиром. Смешивается также со многими другими спиртами и эфирами, ароматическими углеводородами и тетрахлоруглеродом.
Молекула HCN имеет линейное строение с межатомными расстояниями H—C 0,1064 нм и C≡N 0,1156 нм и сильно полярна (электрический дипольный момент μ = 0,992⋅10−29 Кл·м).
Безводный цианистый водород является сильно ионизирующим растворителем, растворённые в нём электролиты хорошо диссоциируют на ионы. Его относительная диэлектрическая проницаемость при 25 °C равна 106,8 (выше, чем у воды). Это обусловлено линейной ассоциацией полярных молекул HCN за счёт образования водородных связей.
Температура плавления −13,29 °C, кипения +25,65 °C. Плотность 0,71618 г/см3 при 0 °C, 0,68708 г/см3 при 0 °C.
Критическое давление 4,95 МПа, критическая температура +183,5 °C, критическая плотность 0,195 г/см3.
Коэффициент преломления nD = 1,26136 (20 °C).
Энтальпия образования 132 кДж/моль, энтальпия плавления 8,41 кДж/моль, энтальпия испарения 25,2 кДж/моль. Энтальпия сгорания −663 кДж/моль. Энтропия 201,71 Дж/(моль·К) (при 298 К).
Динамическая вязкость 0,183 мПа·с, кинематическая вязкость 17,78 мН/м.
Удельное электрическое сопротивление жидкой синильной кислоты 105 Ом·м.
Твёрдая синильная кислота при нормальном давлении существует в двух кристаллических модификациях. При температуре ниже −102,78°C образует кристаллы ромбической сингонии, пространственная группа I2mm, параметры ячейки a = 0,413 нм, b = 0,485 нм, c = 0,434 нм, Z = 2. Выше этой температуры переходит в кристаллы тетрагональной сингонии, пространственная группа I4mm, параметры ячейки a = 0,463 нм, c = 0,434 нм, Z = 2.
Примечания
- ↑
- Обычно под синильной кислотой в химии подразумевается водный раствор цианистого водорода, поэтому отождествление синильной кислоты с самим цианистым водородом, хотя и широко распространено, не вполне корректно.
- ↑ Смирнов С. К. Синильная кислота // Химическая энциклопедия : в 5 т. / Гл. ред. Н. С. Зефиров. — М.: Большая Российская энциклопедия, 1995. — Т. 4: Полимерные—Трипсин. — С. 352. — 639 с. — 40 000 экз. — ISBN 5-85270-039-8.
- . Online Mendelian Inheritance in Man. Дата обращения 31 марта 2010.
- , с. 26.
- , с. 520.
- ↑
- P.Clarke, L.Hardy, A.Williams «Executioners», London, 2008, page 493 (ISBN 978-0-70880-491-9)
- МКХБ Международная организация труда. . www.ilo.org/dyn/icsc/ (2018). Дата обращения 12 ноября 2019.
- Braker W. and A.L. Mossman. Matheson Gas Data Book (англ.). — 6th edition. — Basking Ridge, NJ: Matheson Gas, Lyndhurst, 1980. — 711 p.
Симптомы отравления синильной кислотой (цианидами)
В клинической картине отравлений синильной кислотой выделяют две формы: молниеносную и замедленную.
При действии сверхвысоких доз синильной кислоты развивается: молниеносная, или апоплексическая, форма отравления.
Пострадавший через несколько секунд после воздействия теряет сознание. Развиваются судороги. Кровяное давление после кратковременного подъема падает. Через несколько минут останавливается дыхание и сердечная деятельность.
При замедленной форме развития интоксикации можно выделить несколько периодов:
1) Период начальных проявлений характеризуется легким раздражением слизистых оболочек верхних дыхательных путей и конъюнктивы глаз, неприятным жгуче-горьким вкусом и жжением во рту. Ощущается запах горького миндаля. Наблюдается слюнотечение, тошнота, иногда рвота, головокружение, головная боль, боль в области сердца, тахикардия (иногда брадикардия), учащение дыхания. Нарушается координация движений, ощущается слабость, возникает чувство страха. Перечисленные признаки появляются сразу после воздействия яда. Скрытого периода практически нет.
2) Диспноэтический период (нарушение дыхания) характеризуется мучительной одышкой, резко выраженное увеличение частоты и глубины дыхания. Первоначальное возбуждение дыхания по мере развития интоксикации сменяется его угнетением. Дыхание становится неправильным, с коротким вдохом и длительным выдохом. Нарастает боль и чувство стеснения в груди. Сознание угнетено. Наблюдается выраженная брадикардия, экзофтальм, рвота. Кожные покровы и слизистые приобретают розовую окраску. В легких случаях отравление синильной кислотой этими симптомами и ограничивается. Через несколько часов все проявления интоксикации исчезают.
3) Диспноэтический период может сменяется периодом развития судорог. Судороги носят клонико-тонический нисходящий характер. Сознание утрачивается. Дыхание редкое, кожные покровы и слизистые оболочки розовые. Первоначально наблюдавшееся замедление сердечного ритма с повышением артериального давления в последствии АД становится низким, учащается пульс, становится аритмичным. Развивается острая сердечно-сосудистая недостаточность. Возможна остановка сердца. Все рефлексы снижены. Тонус мышц значительно повышен.
4) Вслед за коротким судорожным периодом, если не наступает смерть, развивается паралитический период. Он характеризуется полной потерей чувствительности, исчезновения рефлексов, расслаблением мышц, непроизвольной дефекацией и мочеиспусканием. Дыхание становится редким, поверхностным. Кровяное давление падает. Пульс частый, слабого наполнения, аритмичный. Развивается кома, в которой пострадавший может находиться до нескольких суток. Температура тела понижена. Цвет венозной крови становится ярко алым. Содержание СО2 в крови снижается, накапливаются недоокисленные продукты обмена веществ: увеличивается содержание молочной кислоты, содержание ацетоновых тел, содержание сахара.
Продолжительность течения всего отравления синильной кислотой (цианидами), как и отдельных периодов интоксикации, колеблется в значительных пределах (от нескольких минут до многих часов). Это зависит от количества яда, попавшего в организм и предшествующего состояния организма. Смерть наступает от остановки дыхания и сердечной деятельности.
Применение
В химическом производстве
Является сырьём для получения акрилонитрила, метилметакрилата, адипонитрила и других соединений. Большое число её производных используются при извлечении благородных металлов из руд, при гальванопластическом золочении и серебрении, в производстве ароматических веществ, химических волокон, пластмасс, каучука, органического стекла, стимуляторов роста растений, гербицидов.
Как отравляющее веществo
Впервые в роли боевого отравляющего вещества синильная кислота была использована французской армией 1 июля 1916 года на реке Сомме. Однако из-за отсутствия кумулятивных свойств и малой стойкости на местности её последующее использование в этом качестве прекратилось.
Синильная кислота являлась основной составляющей препарата «Циклон Б», который был наиболее популярным в Европе во время Второй мировой войны инсектицидом, а также использовался нацистами для убийства людей в концентрационных лагерях. В некоторых штатах США синильная кислота использовалась в газовых камерах в качестве отравляющего вещества при исполнении приговоров смертной казни; в последний раз это было сделано в Аризоне в 1999 году. Смерть, как правило, наступает в течение 5—15 минут.
Применение
В химическом производстве
Является сырьём для получения акрилонитрила, метилметакрилата, адипонитрила и других соединений. Синильная кислота и большое число её производных используются при извлечении благородных металлов из руд, при гальванопластическом золочении и серебрении, в производстве ароматических веществ, химических волокон, пластмасс, каучука, органического стекла, стимуляторов роста растений, гербицидов.
Как отравляющее веществo
Впервые в роли боевого отравляющего вещества синильная кислота была использована французской армией 1 июля 1916 года на реке Сомме . Однако из-за отсутствия кумулятивных свойств и малой стойкости на местности последующее использование синильной кислоты в этом качестве прекратилось.
Синильная кислота являлась основной составной частью препарата «Циклон Б», который применялся нацистами во время Второй мировой войны для убийства людей в концентрационных лагерях. В некоторых штатах США синильная кислота использовалась в газовых камерах в качестве отравляющего вещества при исполнении приговоров смертной казни, в последний раз это было сделано в Аризоне в 1999 году. Смерть, как правило, наступает в течение 5—15 минут.
Соли синильной кислоты называются цианидами. Цианиды подвержены сильному гидролизу. При хранении водных растворов цианидов при доступе диоксида углерода они разлагаются:
Ион CN − (изоэлектронный молекуле СО) входит как лиганд в большое число комплексных соединений d-элементов. Комплексные цианиды в растворах очень стабильны.
Цианиды тяжёлых металлов термически неустойчивы; в воде, кроме цианида ртути (Hg(CN)2), нерастворимы. При окислении цианиды образуют соли — цианаты:
Многие металлы при действии избытка цианида калия или цианида натрия дают комплексные соединения, что используется, например, для извлечения золота и серебра из руд:
Получение
В настоящий момент существуют три наиболее распространённых метода получения синильной кислоты в промышленных масштабах:
Метод .mw-parser-output .ts-comment-commentedText{border-bottom:1px dotted;cursor:help}@media(hover:none){.mw-parser-output .ts-comment-commentedText:not(.rt-commentedText){border-bottom:0;cursor:auto}}Андрусова — прямой синтез из аммиака и метана в присутствии воздуха и платинового катализатора при высокой температуре:
2NH3+2CH4+3O2→Pt2HCN+6H2O.{\displaystyle {\mathsf {2NH_{3}+2CH_{4}+3O_{2}{\xrightarrow {Pt}}2HCN+6H_{2}O}}.}
Метод BMA (Blausäure aus Methan und Ammoniak), запатентованный фирмой Degussa: прямой синтез из аммиака и метана без воздуха в присутствии платинового катализатора при высокой температуре:
NH3+CH4→PtHCN+3H2.{\displaystyle {\mathsf {NH_{3}+CH_{4}{\xrightarrow {Pt}}HCN+3H_{2}}}.}
- Побочный продукт при производстве акрилонитрила путём окислительного аммонолиза пропилена.
- Реакцией цианида калия с водой и диоксидом углерода:
KCN+H2O+CO2⟶HCN+KHCO3{\displaystyle {\mathsf {KCN+H_{2}O+CO_{2}\longrightarrow HCN+KHCO_{3}}}}
Термическим разложением железосинеродистой и железистосинеродистой кислот:
2H3Fe(CN)6 →T FeFe(CN)6+6HCN{\displaystyle {\mathsf {2H_{3}\ {\xrightarrow {T}}\ Fe+6HCN}}}
3H4Fe(CN)6 →100oC Fe2Fe(CN)6+12HCN{\displaystyle {\mathsf {3H_{4}\ {\xrightarrow {100^{o}C}}\ Fe_{2}+12HCN}}}(в присутствии влаги)
В Шавиниганском процессе углеводороды (например, пропан) реагируют с аммиаком. В лаборатории небольшие количества синильной кислоты образуются путём добавления кислот к цианидным солям щелочных металлов:
HCl+NaCN⟶HCN+NaCl{\displaystyle {\ce {HCl + NaCN->HCN + NaCl}}}
H++NaCN⟶HCN+Na+{\displaystyle {\ce {H+ + NaCN ->HCN + Na+}}}
Эта реакция иногда является основой случайных отравлений, потому что кислота превращает нелетучую цианидную соль в газообразный циановодород.
Реакцией монооксида углерода с аммиаком:
NH3+CO→ThO2HCN+H2O.{\displaystyle {\mathsf {NH_{3}+CO{\xrightarrow {ThO2}}HCN+H_{2}O}}.}
Фотолиз метана в бескислородной атмосфере:
2CH4+N2⟶2HCN+3H2{\textstyle {\mathsf {2CH_{4}+N_{2}\longrightarrow 2HCN+3H_{2}}}}
Синильная кислота в судебно-медицинском отношении
Отравления С. к. и цианистыми соединениями сравнительно редки
В основном они носят характер несчастных случаев при неосторожном обращении с ядами в лаб. условиях или в результате употребления в пищу большого количества ядер косточковых плодов (горького миндаля, персиков, слив, абрикосов, черешни)
Абсолютная смертельная доза для человека составляет 40 г горького миндаля или 100 очищенных семян абрикосов, содержащих 1 г амигдалина — алкалоида, легко гидролизующегося на С. к., глюкозу и масло горького миндаля. Встречаются единичные случаи самоубийства и убийства при помощи цианистого калия. Заключение об отравлении как причине смерти основывается на совокупности клин, проявлений и результатов суд.-мед. и лаб. методов исследования. При молниеносной (апоплектиформной) форме отравления С. к. смерть наступает через 3—5 мин., при замедленной несколько позднее.
При осмотре и вскрытии трупа отмечают характерный вишневокрасный цвет трупных пятен, ушных раковин, губ, лица, запах горького миндаля от внутренних органов, красный цвет тканей и внутренних органов, набухание слизистой оболочки желудка. При отравлении ядрами косточковых плодов в желудке обнаруживают непереваренные частицы этих ядер — белые крупинки и коричневые чешуйки оболочки.
Суд.-хим. исследованию подвергают желудок с содержимым, мозг, печень, почку, кровь и мочу. С. к. изолируют из подкисленного биол. материала путем перегонки. Качественное ее обнаружение основано на реакции образования берлинской лазури, количественное — на определении с р-ром азотнокислого серебра или фотоколориметрировании (см. Колориметрия). При спектральном исследовании крови выявляется спектр циангемоглобина. При подозрении на отравление циансодержащими ядрами косточковых плодов проводят ботаническое исследование содержимого желудка и кишечника.
Библиография: Авдеев М. И. Судебно-медицинская экспертиза трупа, с. 371, М., 1976; Бобков С. С. и Смирнов С. К. Синильная кислота, М., 1970; Вредные вещества в промышленности, под ред. Н. В. Лазарева и И. Д. Гадаскиной, т. 3, с. 260, Л., 1977; Лечение острых отравлений, под ред. М. Л. Тараховского, с. 179, Киев, 1982; Лужников Е. А. Клиническая токсикология, с. 189, М., 1982; Профессиональные болезни, под ред. А. А. Летавета и др., М., 1973; Руководство по судебно-медицинской экспертизе отравлений, под ред. Р. В. Бережного и др. с. 141, М., 1980; Справочник по профессиональной патологии, под ред. Л. Н. Грацианской и В. Е. Ковшило, с. 341, Л., 1981; Швайкова М. Д. Токсикологическая химия, с. 69, М., 1975.
Рефераты по химии / Реакции альдегидов и кетонов — присоединение углеродных нуклеофиловСтраница 3
Циановодород присоединяется к альдегидам и кетонам с образованием a-окси-нитрилов ( циангидринов). Сама синильная кислота является очень слабым нуклеофилом и поэтому реагирует очень медленно. С гораздо большей скоростью карбонильная группа реагирует с цианид-ионом.
Альдегиды легко образуют циангидрины. Кетоны с разветвленной цепью углеродных атомов, а также высшие кетоны циангидринов не образуют. Реакцию обычно проводят, прибавляя минеральную кислоту к смеси карбонильного соединения и водного раствора цианида натрия.
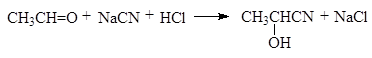 (24)
(24)
2-гидроксипропаннитрил
(ацетальдегидциангидрин)
Гидролизом циангидринов получают a-оксикислоты:
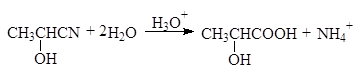 (25)
(25)
нитрил a-оксипро- молочная
пионовой кислоты кислота
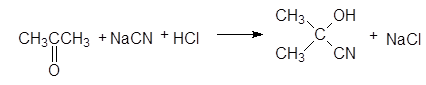 (26)
(26)
ацетонциангидрин
Реакция проходит при щелочном катализе по следующему механизму:
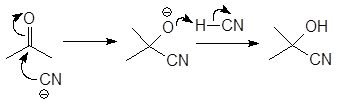 (М 5)
(М 5)
При гидролизе ацетонциангидрина в присутствии соляной кислоты образуется 2-гидрокси-2-метилпропановая кислота, а при его обработке концентрированной серной кислотой – метакриловая кислота:
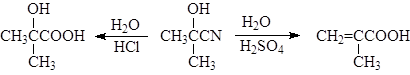 (27,28)
(27,28)
2-гидрокси-2-метилпропановая к-та метакриловая к-та
Ацетонциангидрин широко используется в лабораторной практике для получения других циангидринов, например:
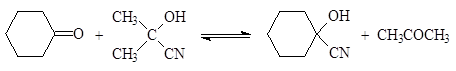 |
(29)
циклогексанонциангидрин
В этой реакции используется обратимость реакций присоединения к карбонильной группе.
Упр.9.
Напишите реакции ацетона и пропионового альдегида с синильной кислотой. Каков механизм этих реакций? Какое из этих соединений и почему будет легче вступать в реакцию? Объясните, почему образование циангидринов ускоряется добавлением оснований, а не добавлением кислот?
Д. Реакция Реформатского
К действию цинкорганических соединений на альдегиды и кетоны сводится реакция Реформатского:
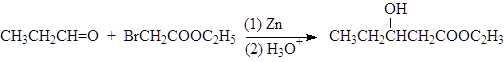 (30)
(30)
пропаналь этилбромацетат этил-3-гидроксивалероат
Упр. 10.
Напишите реакции получения ниже следующих соединений из соответствующих альдегидов и кетонов по реакции Реформатского:
(в)
Страницы: 3
Шееле (Scheele), Карл Вильгельм
Шведский химик Карл Вильгельм Шееле родился в Штральзунде в Померании, которая тогда входила в состав Швеции, в семье пивовара и торговца зерном. Шееле учился в частной школе в Штральзунде, но уже в 1757 г. переехал в Гётеборг. По …
Жолио (Joliot), Жан Фредерик
Французский физик Жан Фредерик Жолио родился в Париже. Он был младшим из шести детей в семье процветающего коммерсанта Анри Жолио и Эмилии (Родерер) Жолио, которая происходила из зажиточной протестантской семьи из Эльзаса. В 1910 …
Создан материал с рекордной фосфоресценцией
Всего через минуту пребывания на солнце новый состав целых две недели довольно ощутимо светится в ближнем инфракрасном диапазоне.
Фосфоресцентные материалы, выдающие видимое излучение после «накачки» светом, широко ра …
Токсичность и биологические свойства
Синильная кислота — сильнейший яд общетоксического действия, блокирует клеточную цитохромоксидазу, в результате чего возникает выраженная тканевая гипоксия. Половинные летальные дозы (LD50) и концентрации для синильной кислоты:
- Мыши:
- перорально (ORL-MUS LD50) — 3,7 мг/кг;
- при вдыхании (IHL-MUS LC50) — 323 м.д.;
- внутривенно (IVN-MUS LD50) — 1 мг/кг.
- Кролики, внутривенно (IVN-RBT LD50) < 1 мг/кг;
- Человек, минимальная опубликованная смертельная доза перорально (ORL-MAN LDLo) < 1 мг/кг.
При вдыхании синильной кислоты в небольших концентрациях наблюдается царапанье в горле, горький вкус во рту, головная боль, тошнота, рвота, боли за грудиной. При нарастании интоксикации уменьшается частота пульса, усиливается одышка, развиваются судороги, наступает потеря сознания. При этом цианоз отсутствует (содержание кислорода в крови достаточное, нарушена его утилизация в тканях).
При вдыхании синильной кислоты в высоких концентрациях или при попадании её внутрь появляются клонико-тонические судороги и почти мгновенная потеря сознания вследствие паралича дыхательного центра. Смерть может наступить в течение нескольких минут.
В организме человека метаболитом синильной кислоты является роданид (тиоцианат) SCN−, образующийся при её взаимодействии с серой под действием фермента роданазы.